一、胃肠道间质瘤是什么疾病
胃肠道间质瘤(GIST)是胃肠道最常见的间叶源性肿瘤(区别于一般的癌症,癌症是胃或肠粘膜的病变,间质瘤都是粘膜下的病变),由突变的c-kit 或血小板源性生长因子受体α (PDGFRA)基因驱动;组织学上多由梭形细胞、上皮样细胞、偶或多形性细胞,排列成束状或弥漫状图像,免疫组化检测通常为CD117或D0G-1表达阳性。
GIST 临床较为少见,发病率约为1/10万~2/10万,占胃肠道肿瘤的2%~3% ,发病部位从食管到肛门皆可出现,而胃和小肠最为多见,60% ~70%发生于胃部,以胃体、胃窦和贲门部多见,20%~30%发生于小肠,结直肠占5%,食管<5%,近年来在肠系膜、网膜、肝脏及女性阴道等处也发现了间质瘤。发病年龄多>40岁,男性多于女性。
其发病原因,总结一句话就是基因的突变,主要是c-kit基因的功能获得性突变,少部分是血小板原性生长因子受体α(PDGFRA)外显子18点突变或缺失。
二、胃肠道间质瘤的常见临床表现
1、消化道出血:
约25% GIST 有消化道出血,由于肿瘤增长过快使血供不足致黏膜缺血、糜烂、溃疡、中心坏死,破溃于胃及肠腔,有报道破裂入腹腔引起腹腔大量出血。
2、腹部隐痛:
腹部隐痛不适,腹痛,部分出现急腹症(溃疡,穿孔)。
3、吞咽困难:
针对食管GIST 的主要表现
4、腹部包块 :
肿瘤外向生长及周围组织浸润,一般比较晚期的表现,早期中期不会出现。
三、如何诊断
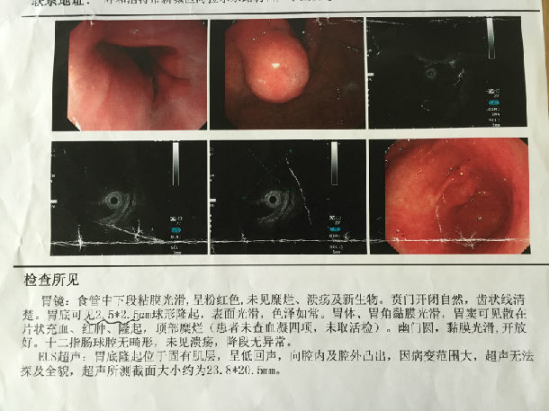
1、内镜检查:对于胃间质瘤诊断手术,最佳检查方式:胃镜检查,可以明确病变位置,大小,有无溃疡及出血;胃镜表现一般是胃粘膜下光滑隆起性病灶。胃镜下考虑是间质瘤,一般会加做超声胃镜。目前超声内镜(EUS) 是监测黏膜下肿瘤的首选方法,可采用超声微探头,也可用标准超声内镜,EUS 可清晰显示病变来源与胃壁各层结构,部位以及病变的大小,形状,边缘和回声等情况。同时,如果考虑是胃间质瘤,一般不取活检病理。一是不容易取到,二是容易出血、肿瘤破裂,导致扩散。除非肿瘤巨大,直接手术切除有困难需要术前服药治疗,必须取活检外,其余不建议取病理活检。
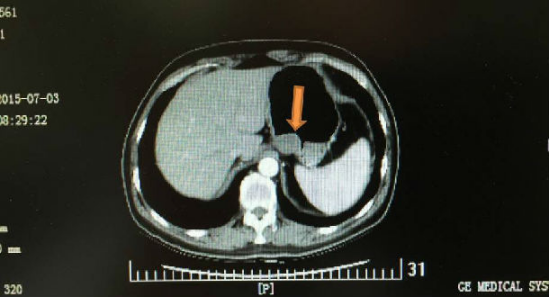
2、影像学检查一般应做:增强腹盆CT或核磁共振成像。
CT表现:GIST多突向腔外生长或沿胃肠壁浸润,大小不等,形态多为分叶状的类圆形肿块,也可为不规则形,大部分边界完整。体积较大的肿块内常见坏死、囊变而显示密度不均。肿块边缘可出现钙化,增强后实性部分多为中度以上强化,病变多数血供丰富,中高度强化,伴瘤周多迂曲供血血管,中央低强化区域对应出血、坏死、囊变、液化。
MRI表现:磁共振成像(MRI) 肿瘤实性部分表现为T1WI低信号,T2WI高信号,增强扫描明显强化。肿瘤内出血区域依据出血时间的长短在T1WI和T2WI 图像中由高信号向低信号变化。MRI T1WI 反相位成像时,组织邻近脂肪间隙的一侧会出现线样无信号区,借助这一特征可辅助判断肿瘤来源于胃肠道或是邻近其他实性脏器。
3、免疫组化检查:
1) 组织学上,依据瘤细胞的形态通常将GIST 分为3 大类:梭形细胞型( 70%) 、上皮样细胞型( 20%)和梭形细胞-上皮样细胞混合型( 10%) 。少数病例可含有多形性细胞,常见于上皮样GIST 内。间质可呈硬化性,尤见于伴有钙化的小肿瘤,偶可呈粘液样。
2) 免疫组化检测CD117 阳性率为94% ~ 98%,DOG1 阳性率为94% ~96%,其中CD117 与DOG1 具有高度一致性。多数梭形细胞GIST( 特别是胃GIST) 表达CD34,但在上皮样GIST 中的表达不一致,在小肠GIST 中CD34 可为阴性。在常规工作中,推荐联合采用上述3 项标记物。需要注意的是,少数非GIST 肿瘤也可表达CD117 和( 或)DOG1,如贲门平滑肌瘤、腹膜后平滑肌瘤、盆腔内平滑肌瘤病、直肠肛管恶性黑色素瘤以及子宫平滑肌肉瘤等,应联合采用其他标记( 如desmin 和HMB45 等) 加以鉴别。此外,免疫组化检测琥珀酸脱氢酶B( SDHB) 有助于识别琥珀酸脱氢酶缺陷型GIST( SDH-deficientGIST)。该型GIST 不表达SDHB,临床上常伴有Carney's 三联征( GIST、副神经节瘤和肺软骨瘤) 或Carney-Stratakis 综合征( 家族性GIST和副神经节瘤),c-kit 或PDGFRA 基因突变检测显示为野生型。
4、基因检测:
基因突变检测十分重要,有助于一些疑难病例的诊断和鉴别诊断、预测分子靶向治疗药物的疗效和指导临床治疗。存在以下情况时,应该进行基因学分析:
1) 对疑难病例应进行c-kit 或PDGFRA突变分析,以明确GIST 的诊断;
2) 术前拟用分子靶向治疗者;
3) 所有初次诊断的复发和转移性GIST,拟行分子靶向治疗;
4) 原发可切除GIST 手术后,中-高度复发风险,拟行伊马替尼辅助治疗;
5) 鉴别NF1型GIST、完全性或不完全性Carney’s三联征、家族性GIST 以及儿童GIST;
6) 鉴别同时性和异时性多原发GIST;
7) 继发性耐药需要重新检测
四、手术治疗
手术治疗原则:手术目标是尽量争取R0 切除。如果初次手术仅为R1 切除,预计再次手术难度低且风险可以控制,不会造成主要功能脏器损伤的患者,可以考虑二次手术。在完整切除肿瘤的同时,应避免肿瘤破裂和术中播散。GIST 很少发生淋巴结转移,除非有明确的淋巴结转移迹象,一般情况下不必行常规清扫。
手术适应症:
对于肿瘤最大径线超过2 cm的局限性GIST,原则上可行手术切除;而不能切除的局限性GIST,或临界可切除,但切除风险较大或严重影响脏器功能者,宜先行术前药物治疗,待肿瘤缩小后再行手术。
对于肿瘤最大径线小于或等于2 cm的可疑局限性GIST,有症状者应进行手术。位于胃的无症状GIST,一旦确诊后,应根据其表现确定超声内镜风险分级(不良因素为边界不规整、溃疡、 强回声和异质性)。如合并不良因素,应考虑切除;如无不良因素,可定期复查超声内镜。位于直肠的GIST,由于恶性程度较高,且肿瘤一旦增大,保留肛门功 能的手术难度相应增大,倾向于及早手术切除。
复发或转移性GIST,分以下几种情况区别对待:①未经分子靶向药物治疗,但估计能完全切除且手术风险不大,可推荐药物治疗或考虑手术切除全 部病灶。② 分子靶向药物治疗有效,且肿瘤维持稳定的复发或转移性 GIST,估计在所有复发转移病灶均可切除的情况下,建议考虑手术切除全部病灶。③局限性进展的复发转移性GIST,鉴于分子靶向药物治疗后总体控制比较 满意,常常只有单个或少数几个病灶进展,可以考虑谨慎选择全身情况良好的患者行手术切除。术中将进展病灶切除,并尽可能切除更多 的转移灶,完成较为满意的减瘤手术。④分子靶向药物治疗下广泛性进展的复发转移性GIST,原则上不考虑手术治疗。 ⑤姑息减瘤手术只限于患者能耐手术并预计手术能改善患者生活质量的情况。
急诊手术适应证:在GIST引起完全性肠梗阻、消化道穿孔、保守治疗无效的消化道大出血以及肿瘤自发破裂引起腹腔大出血时,须行急诊手术。
五、分子靶向药物治疗
(一) GIST术前治疗
1.术前治疗的意义:术前治疗的主要意义:减小肿瘤体积,降低临床分期)缩小手术范围,避免不必要的联合脏器切除,降低手术风险,同时增加根治性切除机会;对于特殊部位的肿瘤,可以保护重要脏器的结构和功能)对于瘤体巨大,术中破裂出血风险较大的患者,可以减少医源性播散的可能性。
2.术前治疗的适应证:(1)术前估计难以达到R0切除;(2)肿瘤体积巨大(大于10 cm),术中易出血、破裂,可能造成医源性播散;(3)特殊部位的肿瘤(如胃食管结合部、十二指肠、低位直肠等),手术易损害重要脏器的功能;(4)肿瘤 虽可以切除,但估计手术风险较大,术后复发率、死亡率较高;(5)估计需要进行多脏器联合切除手术。
3.术前治疗时间、治疗剂量及手术时机选择:对于术前治疗时间,专家委员会尚未获得一致的共识。一般认为,给予伊马替尼术前治疗6个月左右施行手术比较适宜。过度延长术前治疗时间可能会导致继发性耐药。
术前治疗时,推荐伊马替尼的初始剂量为400 mg/d。对于肿瘤进展的患者,应综合评估病情,尚可手术者(有可能完整切除病灶),应及时停用药物,及早手术干预;不能手术者,可以按照复发转移患者采用二线治疗。
4.术前停药时间及术后治疗时间:建议术前停药1周左右,待患者的基本情况达到要求,即可考虑进行手术。术后,原则上只要患者胃肠道功能恢复且能耐 受药物治疗,应尽快进行药物治疗。对于R0切除者,术后药物维持时间可以参考辅助治疗的标准;对于姑息性切除或转移、复发患者 (无论是否达到R0切除),术后治疗与复发转移未手术的GIST患者相似。
(二)GIST 术后辅助治疗
1.辅助治疗适应证:目前推荐有中、高危复发风险患者作为辅助治疗的适合人群。美国外科协会(ASOCOG)Z9001 研究证明,具有复发危险因素的GIST完整切除后,应用伊马替尼辅助治疗1年可明显改善患者的无复发生存率。 国内学者的两项研究也证实,伊马替尼辅助治疗在中高危GIST患者中获益。
2.辅助治疗剂量和时限:根据ASOCOG Z9001以及 SSGXVIII/AIO研究结果,目前推荐伊马替尼辅助治疗的剂量为400 mg/d;治疗时限:对于中危患者,应至少给予伊马替尼辅助治疗1年;高危患者,辅助治疗时间为3年。国内研究提示,中、高危的GIST患者采用伊马替尼辅助治疗3年与单独接受手术患者相比,可以改善3年无复发生存率与总生存期。
(三)转移复发或不可切除GIST的治疗
1.伊马替尼一线治疗
伊马替尼是转移复发或不可切除GIST的一线治疗药物,初始推荐剂量为400 mg/d。 B2222试验结果表明,伊马替尼治疗转移复发GIST的客观疗效高,并且能够明显地改善患者的中位总生存期。
EORTC62005研究中,c-kit外显子9突变患者的初始治疗,应用伊马替尼800mg/d 与 400mg/d比较获得了更长的无进展生存期。推荐初始治疗给予高剂量伊马替尼。 鉴于国内临床实践中多数患者无法耐受伊马替尼800mg/d 治疗,因此,对于c-kit外显子9突变的国人GIST患者,初始治疗可以给予伊马替尼600 mg/d。
对于转移复发或不可切除 GIST, 如伊马替尼治疗有效,应持续用药,直至疾病进展或出现不能耐受的毒性。法国肉瘤协作组的BFR14临床研究,结果表明,中断伊马替尼治疗将导致病情反复,肿瘤快速进展。
2.伊马替尼标准剂量失败后的治疗选择
如果在伊马替尼治疗期间发生肿瘤进展,首先应确认患者否遵从了医嘱, 即在正确的剂量下坚持服药;在除外患者的依从性因素后, 应该参照以下原则处理。
(1)局限性进展:表现为伊马替尼治疗期间,部分病灶出现进展,而其他病灶仍然稳定甚至部分缓解。局限性进展的GIST,在手术可以完整切除局灶进 展病灶的情况下,建议实施手术治疗,术后可继续原剂量伊马替尼或增加剂量治疗。小样本的临床观察提示,局限性进展患者接受肿瘤完整切除术后继续服用伊马替 尼,可以有较好的无疾病进展期与总生存期获益。GIST广泛进展时,不建议采取手术;未能获得完整切除时,后续治疗应遵从 GIST广泛性进展的处理原则。对于部分无法实施手术的 GIST肝转移患者,动脉栓塞与射频消融治疗也可以考虑作为辅助治疗方式;而不宜接受局部治疗的局灶性进展患者,可以增加伊马替尼剂量或者给予舒尼替尼治疗。
(2)广泛性进展:对于应用标准剂量的伊马替尼治疗后出现广泛进展者,建议增加伊马替尼剂量或换用舒尼替尼治疗。①伊马替尼增加剂 量:EORTC62005和S0033研究均显示,对于广泛进展的GIST的患者,增加伊马替尼剂量到800 mg,有1/3的患者可以再次临床获益;2010年NCCN指南第2版指出,可以采用伊马替尼400 mg bid。伊马替尼增加剂量后,有关不良反应会相应增加。我国GIST患者对600mg/d 伊马替尼的耐受性较好,与国外报道800mg/d 剂量的疗效相似。因此推荐国人GIST患者优先增量为600mg/d。②舒尼替尼治疗:A6181004研究显示,对于伊马替尼治疗进展或不能耐受的患者,应用舒尼替尼二线治疗仍然有效,能够改善疾病进展时间和总生存期。舒尼替尼的用药剂量和方式尚缺乏随机对照研究的证据,37.5mg/d 连续服用与 50mg/d (4/2)方案均可选择。
3.伊马替尼与舒尼替尼治疗失败后的维持治疗
伊马替尼与舒尼替尼治疗均进展的GIST患者,建议参加新药临床研究,或者考虑给予既往治疗有效且耐受性好的药物进行维持治疗;也可以考虑使用其他分子靶向药物,如索拉非尼可能有一定的治疗效果,但是需要更多的临床研究证据支持。
六、术后随访
1.术后随访的患者:GIST 手术后最常见的转移部位是腹膜和肝脏,故推荐进行腹、盆腔增强CT或MRI扫描作为常规随访项目。(1)中、高危患者应该每3个月进行CT或MRI检查, 持续3年,然后每6个月1次,直至满5年;(2) 低危患者应每6个月进行CT或MRI检查,持续5年;(3) 由于肺部和骨骼转移的发生率相对较低,建议至少每年1次胸部X线检查,在出现相关症状情况下推荐进行ECT骨扫描。
2.转移复发(或不可切除)或术前治疗患者:(1) 治疗前必须行增强CT作为基线和疗效评估的依据。(2)开始治疗后应至少每3个月随访,复查增强CT或MRI;如果涉及治疗决策,可以适当增加随访次数。(3)治疗初期(前3个月) 的密切监测非常重要,必要时可以行PET-CT扫描确认肿瘤对治疗的反应。(4)必须时应该监测血药浓度变化,指导临床治疗。
