|


【模式生物肿瘤移植】
模式生物肿瘤移植是肿瘤生物学研究中重要的研究方法。肿瘤移植对分析研究细胞恶性、迁移能力尤为重要,而且是鉴定潜在肿瘤干细胞的关键。目前斑马鱼作为移植性肿瘤研究宿主得到一定的发展。从目前取得的成果来看,斑马鱼作为肿瘤移植模型已经在白血病、横纹肌肉瘤和黑色素瘤的研究中体现出明显优势。未来随着图像采集技术和实验技术的发展,斑马鱼肿瘤移植将会在胰腺癌肿瘤生物学的研究显露出更多优势。
多年前研究发现,肿瘤移植进入宿主体内后仍能够保持活性并表现出一定的特征。具有恶性的肿瘤细胞在移植后不仅能够在第一代宿主体内生存,并且能够在连续移植实验后存活。移植已经成为人们广为接受的建立肿瘤模型的方法。此外,移植研究还在药物研究中发挥重要作用,可用于筛选潜在抑制肿瘤恶性的药物和肿瘤治疗方案。

【如何鉴定移植肿瘤细胞的生长能力?】
鉴定移植肿瘤细胞的生长能力已经被用于阐明肿瘤生物学特征,尤其是在恶性、转移性以及肿瘤干细胞的生物活性等重要方面。一项长达50年的研究发现,大多情况下,能在啮齿动物中移植成功的人类肿瘤细胞大多来自于恶性肿瘤患者,而且恶性肿瘤在宿主体内成瘤率也较高。这项研究分析发现肿瘤的恶性是导致其转移的重要原因,能够检测到肿瘤细胞会从注射的位点转移到其他部位并且形成新的肿瘤。除此之外,在啮齿动物模型中移植肿瘤也成为了鉴定肿瘤干细胞类群的重要方法。
肿瘤细胞从单个动物移植到其他动物的一系列行为都反映了肿瘤恶性相关信息。肿瘤细胞可以分离并用于移植,其移植后的增殖需要细胞具有自我更新和繁殖出更多肿瘤细胞的能力。移植研究作为一种分析方法对于检测白血病中具有增殖能力的血瘤细胞,判定其分化为骨髓增生性或是淋巴增殖性疾病发挥了重要作用。从这个意义上讲,移植作为一种分析方法也可以用于区分良性增生和恶性增殖。


【肿瘤细胞移植的实际应用】

对于肿瘤细胞移植后,体内扩散行为的研究也有助于理解迁移、归巢以及血管介导的肿瘤细胞生长特性。肿瘤细胞在小鼠尾静脉注射后会进入血流中,继而可以知道肿瘤细胞的迁移和转移能力。免疫系统抑制的小鼠可作为人源肿瘤细胞移植的合适模型,可以对人源的样本进行同类的研究。异种移植为体内研究人源肿瘤细胞提供了可能性。移植分析也常用于研究斑马鱼固体肿瘤。在斑马鱼体内连续移植再生后得到高侵袭性黑色素瘤细胞,把这些肿瘤细胞移植到透明成鱼体内后可以看到细胞能够从注射位点向远端扩撒,从而能够显示出其转移能力。通过移植斑马鱼RAS诱导的胚胎横纹肌肉瘤也可用于鉴定肿瘤干细胞的类群。
人源肿瘤细胞系能够移植到斑马鱼胚胎中,从而研究肿瘤细胞的恶性、转移性以及对血管新生的作用,这是一种重要的研究方法。很多组实验已经表明,将人源肿瘤细胞系转移到斑马鱼胚胎或者幼鱼中可以诱导血管增生的形成以及内皮细胞基因的表达,这就为研究肿瘤诱发的血管形成提供了一个模型。在囊胚期胚胎斑马鱼中移植能够显示肿瘤细胞是否能够移植成功、侵入和对发育的影响。最近研究表明,荧光标记的胰腺癌细胞和TGFβ刺激转化的人源乳腺上皮细胞(非胰腺癌细胞)在注射到48hpf的胚胎后,都能表现出侵入和转移到其他组织的能力。原位的人源胰腺癌细胞在移植后也能表现出侵入能力,而且可以受到蛋白酶抑制剂处理的调节。这些类型的实验表明斑马鱼可以用来研究和比较不同人源肿瘤细胞的早期血管生成和转移行为。必须要指出的是,目前在成鱼中异种移植还受到一系列因素限制从而不能进行成功的异种移植。成鱼中的免疫组织的作用是主要需要考虑的因素。
肿瘤移植已经在肿瘤细胞生物学研究方面给了我们很多启示。肿瘤的恶性也在不同的肿瘤模型中通过肿瘤在宿主体内的增殖特性而得到揭示。利用荧光标记的转基因品系构建移植模型,已经成功在横纹肌肉瘤中鉴定出富有再生能力的肿瘤干细胞。透明鱼体内进行细胞移植研究发现黑色素瘤能够表现出其迁移能力。此外,研究发现人源肿瘤细胞也能在斑马鱼胚胎中诱导血管形成。这些实验的成功主要借助于斑马鱼作为肿瘤模型系统的优势,能够维持大量样本和构建不同的转基因鱼系,透明成鱼的出现大大推动了斑马鱼在移植实验中的应用。由于肿瘤的分析研究还有很大发展空间,斑马鱼移植性肿瘤模型将会对我们在肿瘤生物学研究中发挥越来越重要的作用。
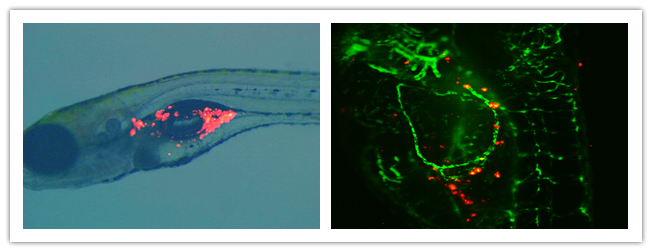
胰腺癌细胞(红色)在斑马鱼体内可以增殖转移,并诱导血管(绿色)生成。
|